ブルセラ症(Brucellosis)
概要
グラム陰性小桿菌であるブルセラ属菌(Brucella spp.)により引き起こされる人獣共通感染症である。ヒツジ、ヤギ、ウシ、ブタなどが主な宿主であり、B. abortus、B. suis、B. melitensis、B. canisの4種がヒトに対して病原性をもつとされる。
ブルセラ症は実験室(検査室)内で最も感染する感染症の一つであり,その感染のしやすさから米国CDCによってカテゴリーBの生物兵器に分類されている。日本では、2023年12月現在、国立感染症研究所バイオセーフティーレベル3に分類されている [1]。
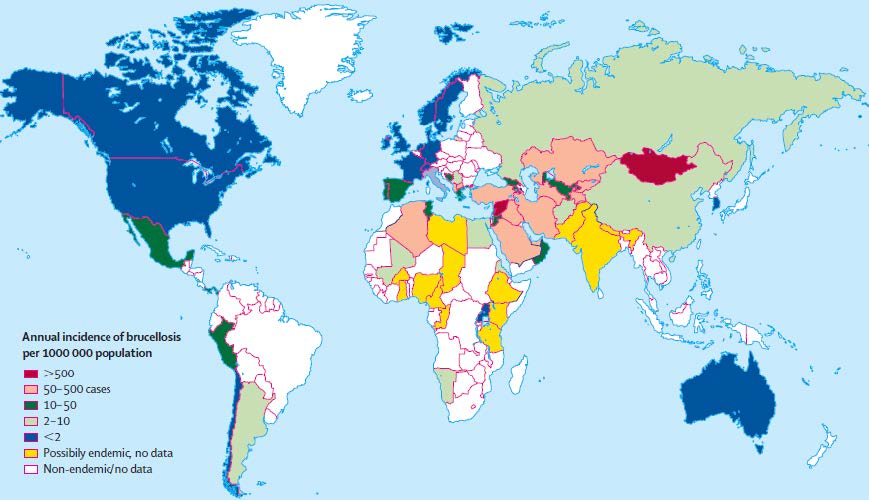
中東や中央アジア、地中海沿岸での報告が多いが、疫学的に明らかではないアフリカにも相応の患者がいることが推測される [2]。
症状
潜伏期間は通常1~4週間であるが、数ヶ月を超えることもある。
急性熱性疾患や慢性感染症として発症し、臨床像は多様である。発熱、関節痛、倦怠感、発汗、など非特異的な症状が多く、発熱は間欠的に繰り返す場合もみられ、リンパ節腫脹や肝脾腫大を呈することもある。
局所合併症としては骨関節症状が多く、特に仙腸関節炎や脊椎椎間板炎、末梢関節炎が一般的である。他にも精巣上体炎や心内膜炎、髄膜脳炎など様々な臓器を侵しうる。
感染経路
ブルセラ菌は非常に感染しやすく10~100個の菌で感染しうる。感染動物の加熱不十分な乳製品の摂取や感染動物の組織(胎盤など)や体液への直接接触、エアロゾル化した菌を吸入することで感染することが多いとされる。ただし、ヒトヒト感染は稀であり、その中でも経胎盤感染や母乳を介した感染報告が多い [3]。
検査
血算、トランスアミナーゼ上昇、炎症反応など非特異的な検査所見のみである。
画像検査ではPedro-Pons signと呼ばれるブルセラ脊椎炎に特徴的な椎体の前上方の溶骨所見がみられることがある。
診断
ブルセラ症の診断は、臨床症状、渡航歴、感染機会の有無を考慮して、培養検査、血清学的検査、PCR検査により確定する。検査材料としては血液、リンパ節生検材料や骨髄穿刺材料、その他、感染巣の組織・体液が利用され、最低21日間の培養を行うことが望ましい。
Haemophilus spp.に似たグラム陰性小桿菌であり、尿や膿などの臨床検体や血液培養陽性検体でこのような菌体が観察された場合には注意をして検査を進める必要がある。質量分析装置のライブラリーにはブルセラ属菌は含まれてはいない。そのため、質量分析で菌種の同定ができなかった検体や、近縁菌のOchrobactrum属菌(すでに一部はBrucella属菌に命名されている)と質量分析あるいは生化学性状で判定された検体ではブルセラ属菌の可能性を考慮して検査を進める必要がある(参照:感染対策)。
ヒトの血清診断では、試験管凝集反応(serum agglutination test, SAT)が行われるが、現在商業ベースでは実施されておらず、行政検査として行われる。PCR検査は分離菌株の同定に有用である。
感染対策
ブルセラ症患者に対する入院中の感染対策は、標準予防策のみで十分である。
検査室での曝露による感染が問題となるため、ブルセラ症が疑われる患者の検体や、通常の同定方法では菌名が特定できないような検体を取り扱う際は、個人防護具を着用してクラスⅡ安全キャビネット内で作業を行い、培養プレートの匂いをかいだり、個人防護具(ガウン、マスク、手袋など)を使用しないといったリスク行為を避けることが重要である。
曝露後のリスク評価
ブルセラ症が発生した場合、曝露者は健康観察や予防内服が推奨される可能性があるため、検査室でブルセラ属菌への曝露者がいないか調査が必要である。調査項目としては、(1)ブルセラ属菌をいつ・誰が取り扱ったか、(2)取り扱った内容(創傷のある皮膚や粘膜への曝露の有無、個人防護具着用の有無、安全キャビネット外での操作の有無、安全キャビネット外でのボルテックス発生手技の有無)、(3)取り扱い時に検査室内に誰がいたかが挙げられる。
曝露状況によって以下の表2のようにリスク分類を行い、曝露後予防の適応を判断する。
表1.ブルセラ症の曝露リスク[4]

曝露後の予防内服とフォローアップ
Minimal riskの場合:曝露後の予防内服は不要である。フォローアップも通常不要であるが、通常の臨床検体(血液、血清、髄液など)を安全キャビネット外で扱った場合や安全キャビネット内であっても適切な防護具なしで扱った場合には症状の経過観察を行うことを考慮する。
Low riskの場合:曝露後の予防内服は不要であるが、免疫不全がある場合や妊婦である場合などケースバイケースで判断を行うこともある。予防内服の有無に関わらずフォローアップは必要であり、曝露後24週間は発熱の有無について健康観察を行う。SATによる血清学的モニタリングを曝露直後(ベースライン)、6週、12週、18週、24週のタイミングで実施する。検査は行政検査として実施するため、自治体の保健所等と相談が必要である。
High risk:曝露後予防としての3週間の予防内服が推奨される。予防内服中は肝機能障害などの副作用に注意し、血液検査のフォローを行う。曝露後24週間の健康観察と血清学的モニタリングについては、Low riskの場合と同様である。
表2.ブルセラ症に対する推奨曝露後レジメン [4]
- ドキシサイクリン 100mg 1日2回内服 + リファンピシン 600mg 1日1回内服 3週間
- ドキシサイクリンまたはリファンピシンが禁忌の場合には、ST合剤を代わりに使用し,ブルセラ属菌に有効な2種類の抗菌薬を投与すべきである。
治療
通常、単剤療法は治療失敗や再発が多いため推奨されず、2剤(テトラサイクリン系+アミノグリコシド系またはリファンピシン)または3剤併用(テトラサイクリン系+アミノグリコシド系+リファンピシン)での治療が推奨されている。表1に、合併症を伴わないブルセラ症に対する一般的な推奨治療レジメンを示す。椎体炎・心内膜炎といった合併症を伴う場合の推奨治療レジメンは成書を参照されたい。
表3. ブルセラ症に対する推奨治療レジメン [5]
- ドキシサイクリン 100 mg 1日2回 内服 6週間 + ゲンタマイシン 5 mg/kg 1日1回 静注/筋注 7-10日間
- ドキシサイクリン 100 mg 1日2回 内服 6週間 + ストレプトマイシン 1 g 1日1回 筋注 2-3週間
- ドキシサイクリン 100 mg 1日2回 内服 6週間 + リファンピシン600-900 mg 1日1回 内服 6週間
保健所への届出
感染症法に基づく4類疾患として、確定症例を診断した場合は、直ちに保健所に報告する義務がある。
参考文献
- 国立感染症研究所. ブルセラ症検査マニュアル第3版. 2023年12月26日閲覧
- Lancet Infect Dis. 2006;6:91-9.
- Trop Med Int Health. 2017;2:539-546.
- Brucellosis Assessing Laboratory Risk Level and PEP. 2023年12月26日閲覧
- Infection. 2021;49:823-832.









